




肖波教授團隊在基于絲素蛋白的納米藥物遞送系統(tǒng)研究方面取得重要進展
來源:家蠶基因組生物學國家重點實驗室
作者:家蠶基因組生物學國家重點實驗室
時間:2021-10-29 09:47:28
近日,肖波團隊在藥學領域重要期刊《Acta Pharmaceutica Sinica B》(IF = 11.4)上發(fā)表了題為“Multi-responsive nanotheranostics with enhanced tumor penetration and oxygen self-producing capacities for multimodal synergistic cancer therapy”的研究性論文。本研究將多種治療功能模態(tài)整合到基于絲素蛋白的納米平臺中,用于腫瘤的協(xié)同治療。在該研究中,該團隊將具有靶向有機陰離子轉運多肽(OATPs)的光敏劑N770共價接枝到負載有抗癌藥物阿霉素(DOX)的絲素蛋白納米粒子表面,獲得多功能納米治療平臺。實驗表明,該治療平臺可以有效靶向到OATPs高表達的惡性腫瘤細胞。同時,具有微晶結構的絲素蛋白納米顆粒顯示出類過氧化氫酶性質,可以緩解腫瘤微環(huán)境的乏氧特性。不僅如此,所獲得的納米粒子N770-DOX@NPs具有明顯的酸性pH、H2O2、GSH和高溫等刺激響應性能,可以響應腫瘤微環(huán)境,實現(xiàn)抗癌藥物的可控持續(xù)釋放,對腫瘤細胞進行持續(xù)的殺傷。小鼠實驗結果表明,在NIR照射下實現(xiàn)了多模態(tài)成像指導下的光動力學療法(PDT)、光熱療法(PTT)和化療協(xié)同治療,顯示出比單一療法更好的治療效果。這種結構簡單,易于構建,同時具有腫瘤靶向、線粒體靶向、多重刺激響應性、多模態(tài)成像、腫瘤微環(huán)境重塑、光療和化療等功能于一體的多功能絲素蛋白納米治療平臺,可以為下一代癌癥靶向協(xié)同治療提供了新的設計思路。
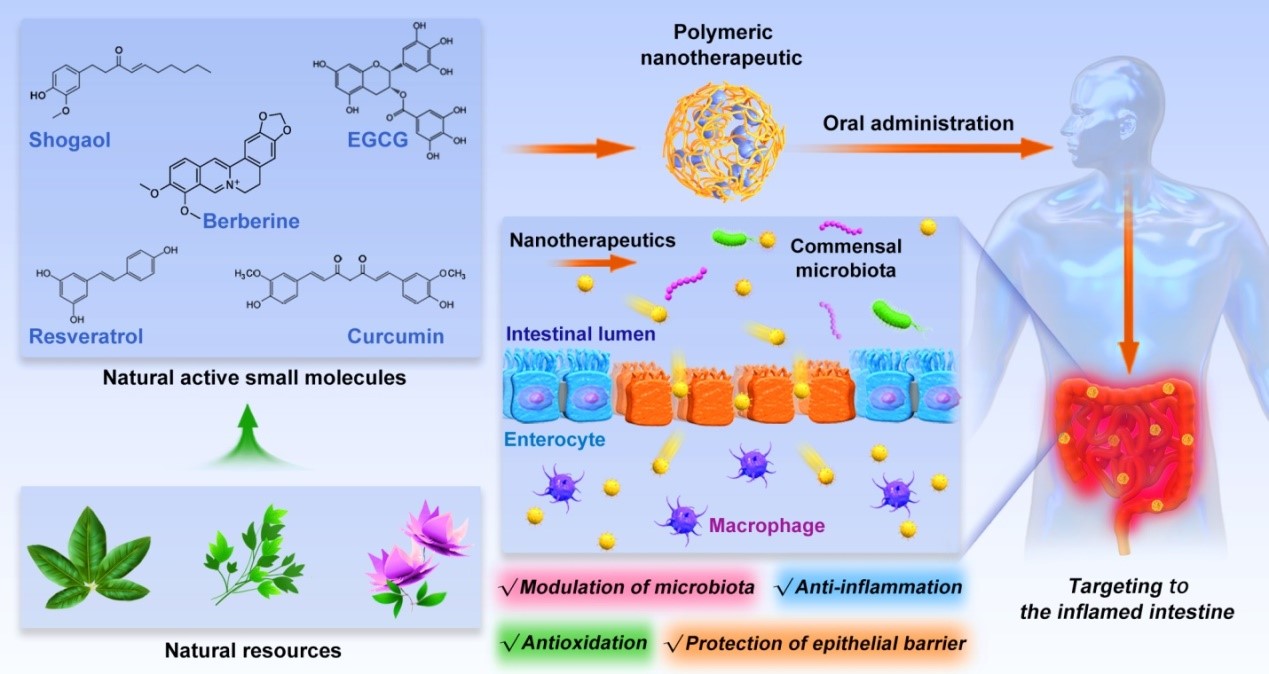
炎癥性腸病(IBD)的全球發(fā)病率呈現(xiàn)急劇上升趨勢,且易轉化為結腸癌。雖然研究人員已經做出了巨大的努力,但仍缺乏根治該疾病的藥物系統(tǒng)。肖波教授受藥物遞送領域重要綜述期刊《Advanced Drug Delivery Reviews》(IF = 15.4)邀請,撰寫題為“Oral delivery of natural active small molecules by polymeric nanoparticles for the treatment of inflammatory bowel diseases”的綜述。該論文對納米藥物系統(tǒng)的載體材料(如絲素蛋白、明膠等)、活性小分子(如白藜蘆醇、姜黃素等)和靶向分子等方面進行了系統(tǒng)的梳理、總結和展望,對未來口服納米藥物系統(tǒng)構建及天然活性小分子藥物的篩選具有重要指導意義。
此外,該團隊最近在植物生物質資源(茶樹花、茶葉)的生物醫(yī)學利用方面同樣取得了重要進展,以“Natural exosome-like nanovesicles from edible tea flowers suppress metastatic breast cancer via ROS generation and microbiota modulation”和“‘Green’ nanotherapeutics from tea leaves for orally targeted prevention and alleviation of colon diseases”為題,分別發(fā)表于《Acta Pharmaceutica Sinica B》(IF = 11.4)和生物材料領域重要期刊《Biomaterials》(IF =12.4)上。
碩士研究生陳秋冰(2016級)、茍雙全(2017級)和俎夢航(2018級)分別為上述論文的第一作者,肖波教授為上述論文的最后通訊作者。家蠶國重室為第2、3、4篇論文的第一署名單位和第1篇論文的合作單位。
這些研究得到了國家自然科學基金(51503172, 81571807和82072060)、中央高校基本業(yè)務費優(yōu)青團隊培育項目、重慶市青年拔尖人才項目和重慶市自然科學基金等項目的支持。
基于在藥物遞送研究方面的積累,肖波教授于2021年5月入選了美國斯坦福大學與Elsevier旗下Mendeley Data聯(lián)合發(fā)布的藥學領域“2020全球前2%頂尖科學家”榜單。
(esilk.net聲明:本網登載此文旨在傳遞更多行業(yè)資訊,文章內容僅供參考。)











